
Le guide de la médecine et de la santé
en Afrique francophone
Suivez-nous :
 Identifiez-vous | Inscription
Identifiez-vous | Inscription

Suivez-nous :
 Identifiez-vous | Inscription
Identifiez-vous | Inscription

Le 3 septembre 1928, le docteur Alexander Fleming, 47 ans, de retour de vacances, retrouve son laboratoire de Saint-Mary's Hospital, à Londres.
Il constate que les boîtes où il faisait pousser des staphylocoques (bactéries) ont été envahies par des colonies cotonneuses d'un blanc verdâtre. C'est qu'elles ont été contaminées par un champignon microscopique, le penicillium notatum, qu'utilisait son voisin de paillasse.
Avant de les jeter, Fleming y jette un coup d'œil et s'aperçoit qu'autour des colonies de champignons, ses staphylocoques ne se sont pas développés ! Il devine qu'une substance sécrétée par le champignon en est responsable et l'appelle aussitôt « pénicilline ». Lire la suite
Elle ne va d’abord servir qu'à isoler en laboratoire la bactérie B. influenzae, qui seule résiste à son action.
En 1936, à Oxford, le professeur Howard Walter Florey engage un biochimiste allemand de 30 ans qui a fui le nazisme, Ernst Boris Chain. Ce dernier pressent l'intérêt de la pénicilline pour la santé humaine et, en mars 1940, réussit à en produire... 100 milligrammes !

Le 25 mai 1940, Florey injecte une dose mortelle de streptocoques à huit souris. Il en traite deux avec une injection de pénicilline et deux autres avec plusieurs injections répétées de pénicilline. Au bout de dix heures, ces dernières survivent ainsi que l'une de celles qui ont reçu une seule dose.
L’équipe publie ses résultats mais l’information tombe à plat. L'Angleterre est bombardée par l'aviation allemande et le public a d'autres préoccupations que les vertus de la pénicilline !
Florey s'embarque donc pour les États-Unis et entre en relation avec une entreprise de l'Illinois, spécialisée dans l'épuration des eaux usées par des bactéries spécialisées.

Un jour, une femme apporte au laboratoire de l'usine un melon recouvert d'une moisissure à l'aspect inhabituel.
Les chercheurs identifient la moisissure : elle a nom penicillium chrysogenum. Et ils découvrent qu'elle produit 200 fois plus de pénicilline que la penicillium notatum ! Il devient dès lors possible de produire la pénicilline à l'échelle industrielle. Les laboratoires américains Merck, Pfizer et Squibb se lancent dans l'aventure.
Première d'une nouvelle famille de médicaments qualifiés d'antibiotiques, la pénicilline va sauver de nombreux blessés sur le front. Elle va ouvrir aussi la voie à la guérison de nombreuses maladies comme la tuberculose ou la syphilis.
On estime que les antibiotiques ont permis de prolonger d'une dizaine d'années l'espérance de vie des hommes. Fleming a été anobli et, en 1945, a reçu le prix Nobel de physiologie-médecine avec Chain et Florey.
Source : herodote.net - Voir la version intégrale
Par Brian J. Werth, PharmD, University of Washington School of Pharmacy - Manuel MSD
Les pénicillines sont des bêta-lactamines des antibiotiques qui sont bactéricides, agissant par des mécanismes inconnus, peut-être en activant des enzymes autolytiques qui détruisent la paroi cellulaire de certaines bactéries.
(Voir aussi Revue générale des médicaments antibactériens.)
Certaines bactéries produisent des bêta-lactamases, qui inactivent les antibiotiques bêta-lactamines; cet effet peut être bloqué par l'ajout d'un inhibiteur des bêta-lactamases.
Toutefois, les inhibiteurs classiques de la bêta-lactamase (p. ex., le clavulanate, le sulbactam et le tazobactam) n'inhibent pas de manière fiable les enzymes suivantes :
De nouveaux inhibiteurs non bêta-lactamines-bêta-lactamases, tels que l'avibactam, le relebactam et le vaborbactam, ont une activité contre l'AmpC, les (Extended-spectrum bêta-lactamases, BLSE) et même certaines carbapénémases telles que les carbapénémases de Klebsiella pneumoniae (KPC), qui sont de plus en plus fréquentes chez Klebsiella spp et d'autres Enterobacterales (précédemment nommées Enterobacteriaceae). Cependant, il n'existe actuellement aucun inhibiteur de bêta-lactamase actif contre les métallo-bêta-lactamases (MBL) telles que les NDM-1 (New Delhi MBL-1), les VIM (Verona integron–encoded MBLs) et les IMP (imipénème) qui peuvent inactiver tous les antibiotiques bêta-lactamines sauf l' aztréonam. Cependant, de nombreuses souches produisant des MBL produisent également d'autres bêta-lactamases capables d'hydrolyser l'aztréonam.
L'alimentation ne perturbe pas l'absorption de l'amoxicilline, mais la pénicilline V doit être administrée 1 heure avant ou 2 heures après un repas. L'amoxicilline a généralement remplacé l'ampicilline en utilisation orale, car elle est mieux absorbée, elle entraîne moins d'effets indésirables gastro-intestinaux et peut être administrée moins fréquemment.
Les pénicillines diffusent rapidement dans le liquide extra-cellulaire de la majorité des tissus, en particulier en cas d'inflammation.
Toutes les pénicillines sont au moins partiellement excrétées par voie rénale et la plupart atteignent des taux élevés dans l'urine. La pénicilline G parentérale est rapidement excrétée (demi-vie sérique de 0,5 heure), sauf en ce qui concerne les formes retard (sels de pénicilline G benzathine ou procaïne); ces formes sont destinées aux injections profondes IM uniquement et entraînent un dépôt de substance à partir duquel la résorption a lieu pendant plusieurs heures à plusieurs jours. La pénicilline benzathine atteint son maximum plus lentement et agit généralement plus longtemps que la pénicilline procaïne. Les sels de procaïne ont une biodisponibilité accrue, ce qui entraîne une élimination plus rapide du médicament; par exemple, la pénicilline G procaïne ne peut être détectée dans le sang que pendant 1 semaine par rapport à la pénicilline G benzathine, qui peut être détectée pendant 30 jours (1).
Référence pour la pharmacocinétique
1. Centers for Disease Control and Prevention (CDC): Inadvertent use of Bicillin C-R to treat syphilis infection—Los Angeles, California, 1999-2004. MMWR Morb Mortal Wkly Rep 54(9):217–219, 2005. PMID: 15758893
Les médicaments similaires à la pénicilline G (y compris la pénicilline V) sont principalement utilisés contre :
Une minorité de bacilles Gram négatifs est également sensible à de fortes doses parentérales de pénicilline G. La plupart des staphylocoques, la plupart des Neisseria gonorrhoeae, de nombreux bacilles anaérobies Gram négatifs et près de 30% des Haemophilus influenzae sont résistants.
La pénicilline G est le médicament de choix pour le traitement de la syphilis, de certaines infections clostridiales et, associée à la gentamicine, de l' endocardite à entérocoques sensibles
La benzathine pénicilline G est une formulation à action prolongée, disponible en tant que :
Parmi les 3 produits, seule la benzathine pénicilline pure est recommandée dans le traitement de la syphilis, ainsi qu'en prévention d'un rhumatisme articulaire aigu. La benzathine pénicilline et le mélange en quantités égales sont indiqués dans le traitement des infections des voies respiratoires supérieures ainsi que dans le traitement des infections cutanées et des tissus mous provoquées par les streptocoques sensibles.
Ces médicaments sont plus actifs contre :
L'adjonction d'un inhibiteur de bêta-lactamase (clavulanate ou sulbactam) permet de l'utiliser contre les staphylocoques sensibles à la méthicilline, H. influenzae, Moraxella catarrhalis, Bacteroides spp, E. coli et K. pneumoniae.
L''ampicilline est indiquée essentiellement pour des infections en général provoquées par les bactéries Gram négatives sensibles :
Ces médicaments (dicloxacilline, nafcilline, cloxacilline, flucloxacilline et oxacilline) sont principalement utilisés pour Staphylococcus aureus producteur de pénicillinase et sensible à la méthicilline Ces médicaments sont également utilisés dans certaines infections à Streptococcus pneumoniae, streptocoques du groupe A et dans des infections à staphylocoque coagulase négatif sensible à la méthicilline.
La pipéracilline et la pipéracilline/tazobactam ont une activité contre :
L'ajout d'un inhibiteur des bêta-lactamases augmente l'activité contre les microrganismes producteurs de bêta-lactamases des espèces S. aureus, E. coli, K. pneumoniae, H. influenzae, sensibles à la méthicilline, et les bacilles Gram négatifs anaérobies, mais pas contre les bacilles Gram négatifs qui produisent une bêta-lactamase AmpC ou une KPC et ne peut inhiber que partiellement les bêta-lactamases à spectre étendu produites par certains K. pneumoniae, E. coli et d'autres Enterobacterales (précédemment nommées Enterobacteriaceae). Les pénicillines à large spectre présentent une synergie avec les aminosides et sont habituellement associées à cette classe pour traiter les infections à P. aeruginosa.
Les pénicillines sont contre-indiquées chez les patients chez qui elles ont provoqué de graves réactions allergiques.
Les pénicillines sont parmi les antibiotiques les plus sûrs pendant la grossesse. Les études sur la reproduction animale effectuées avec la pénicilline n'ont pas montré de risque pour le fœtus. Les données relatives à la grossesse chez la femme sont limitées. Si elles sont indiquées médicalement, les pénicillines peuvent être utilisées pendant la grossesse. La pénicilline G permet de prévenir la transmission maternelle de la syphilis au fœtus et les infections fœtales et maternelles.
Les pénicillines passent dans le lait maternel en petites quantités. Leur prise est habituellement considérée comme compatible avec l'allaitement.
Les effets indésirables des pénicillines comprennent :
D'autres effets indésirables se produisent plus rarement.
La pénicilline orale peut provoquer une langue chevelue noire, qui est due à l'irritation de la surface glossale et à la kératinisation des couches superficielles. C'est une maladie rare et inoffensive qui disparaît après l'arrêt du médicament.
La plupart des effets indésirables sont des réactions d'hypersensibilité :
La plupart des patients qui signalent une réaction allergique à la pénicilline ne réagissent pas à une exposition ultérieure à la pénicilline. Bien que faible, le risque de réaction allergique est près de 10 fois plus élevé chez les patients qui ont un antécédent de réaction allergique. De nombreux patients rapportent des effets indésirables à la pénicilline qui ne sont pas réellement de nature allergique (p. ex., effets indésirables gastro-intestinaux, symptômes non spécifiques).
Si les patients ont un vague antécédent d'allergie ou une histoire incohérente d'allergie à la pénicilline et que l'alternative thérapeutique risque d'être inefficace ou peu adaptée, des tests cutanés peuvent être pratiqués. Une désensibilisation peut être tentée chez les patients qui présentent un test cutané positif en l'absence d'alternative à un médicament de type pénicilline. Cependant, les patients qui ont des antécédents d'anaphylaxie à la pénicilline ne doivent pas recevoir d'autres pénicillines ou des bêta-lactamines ayant des chaînes latérales similaires (y compris pour les tests cutanés), sauf dans de très rares circonstances où aucun substitut ne peut être trouvé et si le médicament peut être administré sous surveillance dans un environnement contrôlé. Dans de tels cas, des précautions et des protocoles de désensibilisation particuliers sont nécessaires.
On observe des exanthèmes plus souvent avec l'ampicilline et l'amoxicilline qu'avec les autres pénicillines. Les patients qui présentent une mononucléose infectieuse développent souvent une éruption non allergique, habituellement maculopapuleuse, débutant habituellement entre le 4e et le 7e jour du traitement.
Les pénicillines peuvent également provoquer :
La leucopénie semble être le plus souvent due à la nafcilline. Toute pénicilline à très forte dose IV peut perturber la fonction plaquettaire et provoquer des hémorragies.
D'autres effets indésirables comprennent des douleurs au point d'injection IM, une thrombophlébite lorsque plusieurs doses IV sont administrées sur le même site d'injection et des troubles gastro-intestinaux avec les administrations orales.
La ticarcilline et la carbénicilline à fortes doses peuvent provoquer une surcharge en sodium, en particulier chez les patients insuffisants cardiaques ou rénaux, car ce sont tous deux des sels disodiques. La ticarcilline et la carbénicilline peuvent également provoquer une alcalose métabolique hypokaliémique parce que la grande quantité d'anion non résorbable présentée aux tubules distaux modifie l'excrétion des ions H+ et secondairement induit une perte de potassium.
Les pénicillines, à l'exception des pénicillines antistaphylococciques (p. ex., nafcilline, oxacilline, cloxacilline, dicloxacilline), atteignant des taux élevés dans l'urine, les doses doivent être réduites en cas d'insuffisance rénale sévère. Le probénécide inhibe la sécrétion tubulaire rénale de nombreuses pénicillines, augmentant les taux sanguins. Il est parfois administré simultanément pour maintenir des taux sanguins élevés.
Source : Pénicillines par Brian J. Werth, PharmD, University of Washington School of Pharmacy
M. Daou, H. Hamidou Issa, S. Moussa, A.M. Gado, M. Ide, M. Baragé Magoudani, Y. Hanki, M. Doutchi, E.O. Adéhossi - Niger. Publié dans Médecine d'Afrique Noire - N° 7006 - Juin 2023 - pages 357-363 - Lire l'article
K. Ravahatra, R.A. Rakotondrabe, Z.A. Razafindrasoa, J. Rakotomizao H.M. Tiaray, J.L. Rakotoson, R.N. Raharimanana - Madagascar. Publié dans Médecine d'Afrique Noire - N° 7002 - Février 2023 - pages 103-111 - Lire l'article
N. Akimana, S. Moumbe Tamba, V. Barendegere - Burundi. Publié dans Médecine d'Afrique Noire - N° 6906 - Juin 2022 - pages 363-371 - Lire l'article
H. Kafando, K. Ouattara, M. Sawadogo, A. Ouedraogo, L. Sangare - Burkina Faso. Publié dans Médecine d'Afrique Noire - N° 6812 - Décembre 2021 - pages 729-737 - Lire l'article
M. Ndiaye, M. Jalloh, O. Boye, N.M. Thiam, A.H. Mbaye, N.N. Diouf, Y. Dia, S.T. Faye, M. Ndoye, I. Labou, L. Niang, M. Niang, S.M. Gueye - Sénégal. Publié dans Médecine d'Afrique Noire - N° 6803 - Mars 2021 - pages 171-178 - Lire l'article
S.Y.E. Houndonougbo, Y. Gerosa, S.R. Tobome, R. Akpata, H. Abdou Lassissi, R. Aholou, D. Kouma, C.H.E. Bankole, N. Yotto - Bénin. Publié dans Médecine d'Afrique Noire - N° 6211 - Novembre 2015 - pages 547-548 - Lire l'article
D. Amoussou-Guenou, F.A. Wanvoegbe, E. Boko, J. Segnon-Agueh, K.A. Agbodande, A. Kerekou, F. Djrolo - Bénin. Publié dans Médecine d'Afrique Noire - N° 6205 - Mai 2015 - pages 241-246 - Lire l'article
B. Ramilitiana, RA Rakotoarivelo, SH Razafimahefa, D Vololontiana, A Randrianarison, MJD Randria , WFH Randriamarotia - Madagascar. Publié dans Médecine d'Afrique Noire - N° 6110 - Octobre 2014 - pages 514-518 - Lire l'article
A. R. Koffi, T. Ouassa, A. Dadie, T. Karou, M. Dje Koffi - Côte d'Ivoire. Publié dans Médecine d'Afrique Noire - N° 5906 - Juin 2012 - pages 336-342 - Lire l'article
Dia D, Seck A, Mbengue M, Diouf ML, Bassène ML, Fall S, Halim A, Breurec S - Sénégal. Publié dans Médecine d'Afrique Noire - N° 5811 - Novembre 2011 - pages 503-507 - Lire l'article
Ouedraogo A-S, Dakoure PWH, Coulibaly S, Sanon BG, Cessouma R, Poda GEA, Nacro B - Burkina Faso. Publié dans Médecine d'Afrique Noire - N° 5801 - Janvier 2011 - pages 36-40 - Lire l'article
A. Toure Ecra, Kone Sayon, A. Horo, M. Fanny, R. Konan Ble, M. Kone - Côte d'Ivoire. Publié dans Médecine d'Afrique Noire - N° 5702 - Février 2010 - pages 81-89 - Lire l'article
A. BAITE, A. MEJDANE, A. NAITHLOU, O. LAGHZAOUI, M. AZENNAG, PH. KOUNA, ELS BONGO ONDIMBA - Gabon. Publié dans Médecine d'Afrique Noire - N° 5207 - Juillet 2005 - pages 403-406 - Lire l'article
K. N'GUESSAN, S. BONI, D. GONDO, M. BOKOSSA, Y. DOUMBIA, N. KONE, K. BOHOUSSOU - Côte d'Ivoire. Publié dans Médecine d'Afrique Noire - N° 5102 - Février 2004 - pages 73-77 - Lire l'article
Z. TARNAGDA, S. DIAGBOUGA, P. SANKARA, K. KIENOU, S. YARO, P. VAN DE PERRE - Burkina Faso. Publié dans Médecine d'Afrique Noire - N° 4804 - Avril 2001 - pages 141-144 - Lire l'article
Par Brian J. Werth, PharmD, University of Washington School of Pharmacy - Manuel MSD
Les céphalosporines sont des antibiotiques bêta-lactamines bactéricides. Elles inhibent les enzymes de la paroi cellulaire des bactéries sensibles, perturbant la synthèse de la paroi cellulaire. Il existe 5 générations de céphalosporines.
(Voir aussi Revue générale des médicaments antibactériens.)
Les céphalosporines pénètrent bien dans la plupart des liquides corporels et le liquide extra-cellulaire de la plupart des tissus, en particulier en présence d'une inflammation (qui favorise la diffusion). Cependant, les seules céphalosporines qui atteignent des niveaux assez élevés dans le liquide céphalorachidien pour traiter une méningite sont les suivantes :
Toutes les céphalosporines pénètrent mal dans le liquide intracellulaire et le corps vitré.
La plupart des céphalosporines sont principalement éliminées par voie urinaire, de sorte que leur posologie doit être adaptée en cas d'insuffisance rénale. La céfopérazone et la ceftriaxone, qui ont une élimination biliaire importante, ne nécessitent pas d'ajustement de la posologie.
Les céphalosporines sont bactéricides pour la plupart des bactéries suivantes :
Les céphalosporines sont classées en générations (voir tableau Certaines des utilisations cliniques des céphalosporines de 3e et 4e génération). Les médicaments de 1ère génération sont efficaces surtout contre les microrganismes Gram positif. Les générations les plus récentes présentent généralement un large spectre contre les bacilles aérobies Gram négatif. Les céphalosporines de 5e génération, céftaroline et ceftobiprole, sont actives contre Staphylococcus aureus résistant à la méthicilline. Les céphalosporines ont les limitations suivantes :
Ces médicaments présentent une excellente activité contre Cocci Gram positifs.
Les céphalosporines orales de 1ère génération sont fréquemment utilisées dans les infections cutanées et des tissus mous non compliquées, dues habituellement à des staphylocoques et à des streptocoques.
La céfazoline par voie parentérale est fréquemment utilisée en cas d' endocardite à S. aureus sensible à la méthicilline et en prophylaxie en chirurgie cardiothoracique, orthopédique, abdominale et pelvienne.
Les céphalosporines de seconde génération sont actives contre :
Les céphamycines sont des médicaments qui ont été initialement produits par Streptomyces mais sont à présent synthétiques. Elles sont généralement classés avec les céphalosporines de 2e génération. Les céphamycines sont plus actives contre les anaérobies, telles que Bacteroides spp, y compris Bacteroides fragilis.
Ces médicaments peuvent être légèrement moins actifs contre les cocci Gram positif que les céphalosporines de 1ère génération. Les céphalosporines de 2e génération et les céphamycines (céfoxitine et céfotétan) sont souvent utilisées en cas d'infections polymicrobiennes impliquant des bacilles Gram négatifs et des cocci Gram positifs. Comme les céphamycines sont actives contre Bacteroides spp, elles peuvent être utilisées lorsque des microrganismes anaérobies sont suspectés (p. ex., sepsis abdominal, ulcères de décubitus, ou infections du pied diabétique). Cependant, dans les certains hôpitaux, ces bacilles ne sont plus régulièrement sensibles aux céphamycines.
Ces médicaments sont actifs contre Haemophilus influenzae et certaines Enterobacterales (précédemment nommées Enterobacteriaceae, p. ex., Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis) non producteurs de bêta-lactamases AmpC ou de bêta-lactamases à spectre étendu.
La plupart des céphalosporines de 3e génération, dont la ceftriaxone et le céfotaxime, sont également actives contre certaines espèces à Gram positif, notamment les streptocoques, dont certaines souches à sensibilité réduite à la pénicilline. La céfixime et le ceftibutène par voie orale sont peu actifs contre S. aureus et, leur utilisation dans les infections de la peau et des tissus mous, doit être limitée aux infections streptococciques non compliquées.
La ceftazidime et la céfopérazone sont actives contre Pseudomonas aeruginosa, alors que le reste de la classe ne l'est pas. Toutes deux sont également actives contre Streptococcus spp et staphylocoques sensibles à la méthicilline. L'ajout d'avibactam au ceftazidime augmente son spectre et permet d'inclure les Enterobacterales produisant de l'AmpC, des bêta-lactamases à spectre étendu ou la carbapénémase de Klebsiella pneumoniae (KPC).
Ces céphalosporines (notamment les céphalosporines de 4e génération) ont de nombreuses utilisations cliniques (voir tableau Certaines des utilisations cliniques des céphalosporines de 3e et 4e génération).
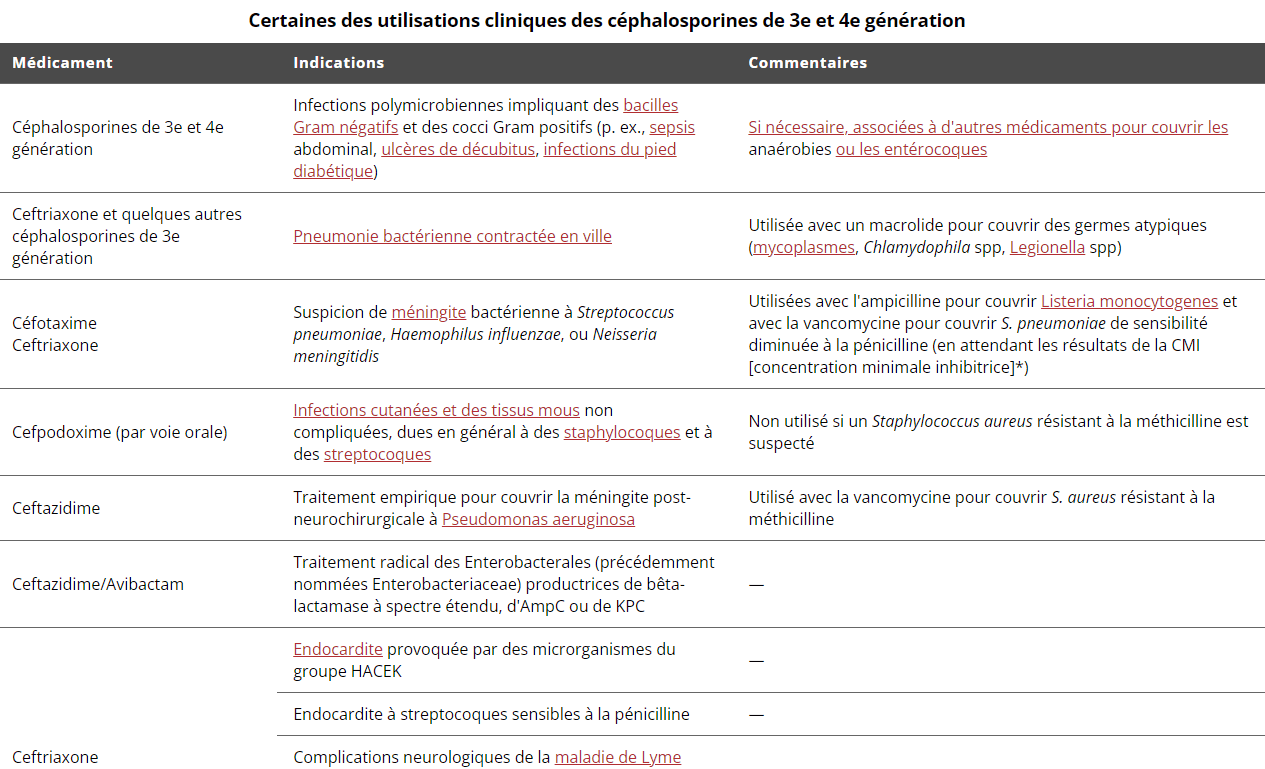
Le céfépime (céphalosporine de 4e génération) est actif contre :
Le ceftobiprole (céphalosporines de 5e génération) et de ceftobiprole sont actifs contre :
Leur activité contre d'autres cocci Gram-positif et d'autres bacilles Gram-négatif est similaire à celle des céphalosporines de 3e génération. Les céphalosporines de 5e génération ne sont pas actives contre Pseudomonas spp.
Les céphalosporines sont contre-indiquées en cas d'antécédents d'hypersensibilité majeure à d'autres céphalosporines. La réactivité croisée avec les pénicillines et d'autres classes de bêta-lactamines, dont d'autres céphalosporines, est moins fréquente qu'on ne le pensait, en particulier chez les patients qui ont eu des réactions bénignes (non anaphylactiques) aux pénicillines. Environ 2% des patients allergiques à la pénicilline ont une réactivité croisée avec les céphalosporines (1, 2). La sensibilité croisée avec l'allergie à la pénicilline n'est pas la même pour toutes les céphalosporines, elle dépend de caractéristiques chimiques et structurelles spécifiques. L'utilisation de céphalosporines de 3e ou 4e génération ou de céphalosporines avec des chaînes latérales R1 différentes de celles de la pénicilline présente un risque négligeable d'allergie croisée; la céfazoline, en particulier, a une chaîne latérale unique et une très faible réactivité croisée. Cependant, les patients qui ont une allergie aux antibiotiques sont un peu plus susceptibles de réagir à un autre antibiotique, les céphalosporines doivent donc être administrées avec prudence aux patients qui ont eu une réaction allergique importante à d'autres bêta-lactamines (3, 4, 5).
La ceftriaxone est contre-indiquée dans les cas suivants :
Références pour les contre-indications :
Les céphalosporines sont généralement considérées comme sans danger pendant la grossesse. Aucune étude n'a montré de risque pour le fœtus humain, mais aucune étude prospective rigoureuse n'a été réalisée.
Les céphalosporines passent dans le lait maternel et peuvent modifier le microbiote intestinal du nourrisson. Ainsi, leur utilisation pendant l'allaitement est souvent déconseillée.
Les effets indésirables significatifs potentiels des céphalosporines comprennent :
Les réactions d'hypersensibilité sont les effets indésirables systémiques les plus fréquents; les éruptions cutanées sont fréquentes, mais l'urticaire et l'anaphylaxie sont rares (réactions médiées par les IgE).
L'allergie croisée entre céphalosporines et pénicillines est rare; les céphalosporines peuvent être administrées avec prudence en cas de besoin à des patients qui ont des antécédents d'hypersensibilité retardée à la pénicilline. Des douleurs au point d'injection IM et une thrombophlébite après injection IV sont possibles.
Le céfopérazone peut avoir un effet antabuse (disulfirame) et en cas d'ingestion d'alcool, entraîner des nausées et des vomissements. Le céfotétan peut aussi augmenter le temps de prothrombine (temps de Quick [TQ])/INR et le temps partiel de thromboplastine (= TPP, TCK, TCA, TPP), un effet réversible sous vitamine K.
D. Kone, J. Kadiané-Oussou, S. Kone, M.T Yapo, J.M. Karidioula, F. Koné, K.G.R. Kouamé, Y.T. Aba, O. Kra - Côte d'Ivoire. Publié dans Médecine d'Afrique Noire - N° 7003 - Mars 2023 - pages 182-190 - Lire l'article
K. Ravahatra, R.A. Rakotondrabe, Z.A. Razafindrasoa, J. Rakotomizao H.M. Tiaray, J.L. Rakotoson, R.N. Raharimanana - Madagascar. Publié dans Médecine d'Afrique Noire - N° 7002 - Février 2023 - pages 103-111 - Lire l'article
H. Kafando, K. Ouattara, M. Sawadogo, A. Ouedraogo, L. Sangare - Burkina Faso. Publié dans Médecine d'Afrique Noire - N° 6812 - Décembre 2021 - pages 729-737 - Lire l'article
M. Ndiaye, M. Jalloh, O. Boye, N.M. Thiam, A.H. Mbaye, N.N. Diouf, Y. Dia, S.T. Faye, M. Ndoye, I. Labou, L. Niang, M. Niang, S.M. Gueye - Sénégal. Publié dans Médecine d'Afrique Noire - N° 6803 - Mars 2021 - pages 171-178 - Lire l'article
B. Ramilitiana, RA Rakotoarivelo, SH Razafimahefa, D Vololontiana, A Randrianarison, MJD Randria , WFH Randriamarotia - Madagascar. Publié dans Médecine d'Afrique Noire - N° 6110 - Octobre 2014 - pages 514-518 - Lire l'article
O. KRA, DA KASSI, T. ABA, E. BISSAGNENE, A. KADIO - Côte d'Ivoire. Publié dans Médecine d'Afrique Noire - N° 5409 - Août/Sept. 2007 - pages 429-432 - Lire l'article
A.L. ROBINSON, R.H. RAJAONARISON, L. RAVELOMANANA, N. RABESANDRATANA, N. RAVELOMANANA - Madagascar. Publié dans Médecine d'Afrique Noire - N° 5407 - Juillet 2007 - pages 391-395 - Lire l'article
M.J. TANON-ANOH, D. SANOGO, M. KOUASSI, M. FOLOQUET-AMORISSANI, A. KACOU-N’DOUBA, E. ETTE-AKRE, A. MANDAH-ANGUI, B. KOUASSI - Côte d'Ivoire. Publié dans Médecine d'Afrique Noire - N° 5303 - Mars 2006 - pages 176-181 - Lire l'article


Betazidim® injectable.
Ceftazidime USP équivalent à Ceftazidime 1 g de poudre sèche.
Poudre pour injection IV ou IM.
La posologie usuelle chez l'adulte est de 1 g toutes les 8 à 12 heures, par voie intraveineuse ou intramusculaire.
La posologie dépend de la sensibilité des germes en cause, de la gravité de l'infection, de l'état général et la fonction rénale du patient.
La clairance rénale de le ceftazidime est diminuée chez les personnes âgées. Par conséquent, il est recommandé de ne pas dépasser la dose maximale de 3 g par jour chez les patients de plus de 80 ans.
D'après les données disponibles, un ajustement posologique n'est pas nécessaire en cas d'insuffisance hépatique légère ou modérée. Il n'y a pas de données issues d'études chez les patients ayant une insuffisance hépatique sévère. Un suivi régulier de l'efficacité et de la tolérance du traitement est conseillé.
La ceftazidime est éliminée dans les urines sous forme inchangée. Par conséquent, la dose doit être diminuée chez les patients ayant une insuffisance rénale.
Hypersensibilité.
Hypersensibilité, colite pseudomembraneuse, fonction rénale, émergence de germes résistants.
Catégorie B.
Les effets indésirables les plus courants sont : éosinophilie, thrombocytose, phlébite thrombophlébite en administration intraveineuse, diarrhée, élévation transitoire des enzymes hépatiques, urticaire ou éruption maculopapuleuse, douleur et/ou inflammation consécutive l'injection intramusculaire, test de Coomb positif.
Antibactériens. Code ATC : J01DD02
Boîte de 1 flacon de poudre + eau pour injection.
Liste I
Strides Pharma Science Limited
Strides House, Opp IIM-B, Bilekahalli,
Bannerghatta Road,
Bangalore – 560076, India
Février 2019.
Dernière mise à jour de cette page
12/06/2019.
![]() Adresse
Adresse
![]() Téléphone
Téléphone
Revue MAN
Revue OST
Actualités
Webinaires
Espaces labos