
Le guide de la médecine et de la santé
en Afrique francophone
Suivez-nous :
 Identifiez-vous | Inscription
Identifiez-vous | Inscription

Suivez-nous :
 Identifiez-vous | Inscription
Identifiez-vous | Inscription
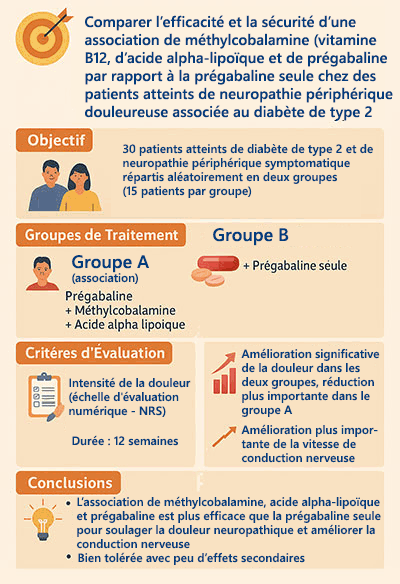
Vasudevan D, Naik MM, Mukaddam QI. Efficacy and safety of methylcobalamin, alpha lipoic acid and pregabalin combination versus pregabalin monotherapy in improving pain and nerve conduction velocity in type 2 diabetes associated impaired peripheral neuropathic condition. [MAINTAIN]: Results of a pilot study. Ann Indian Acad Neurol 2014;17:19-24. Received: 26-07-13, Revised: 10-10-13, Accepted: 16-10-13
Cette étude conclut que l'association méthylcobalamine + acide alpha-lipoïque + prégabaline est plus efficace que la prégabaline seule pour soulager la douleur neuropathique et améliorer la conduction nerveuse.
Bien tolérée, cette stratégie combinée pourrait représenter une option thérapeutique prometteuse pour les patients atteints de neuropathie diabétique périphérique douloureuse.
Comparer l'efficacité et la tolérance d'une association de trois molécules : méthylcobalamine (vitamine B12), acide alpha-lipoïque et prégabaline, contre la prégabaline seule chez des patients atteints de neuropathie périphérique douloureuse liée au diabète de type 2.
30 patients adultes atteints de diabète de type 2 avec neuropathie périphérique symptomatique répartis aléatoirement en deux groupes égaux (15 patients par groupe).
Les deux traitements ont été administrés deux fois par jour, par voie orale, pendant une période de 12 semaines.
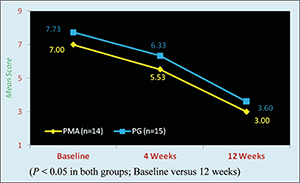
L'ajout de méthylcobalamine et d'ALA à la prégabaline dans le traitement de la neuropathie douloureuse diabétique réduit la douleur, aide à réparer la fonction nerveuse et diminue le stress oxydatif.
L’association méthylcobalamine + acide alpha-lipoïque + prégabaline est plus efficace que la prégabaline seule pour :
Bien tolérée, cette stratégie combinée pourrait représenter une option thérapeutique prometteuse pour les patients atteints de neuropathie diabétique périphérique douloureuse.
Nécessité de confirmer les résultats par une étude plus large.
Consulter cette étude en texte intégral (PDF - anglais)
X. Moisset, D. Bouhassira, J. Avez Couturier, H. Alchaar, S. Conradi, M.-H. Delmotte, M. Lantéri-Minet, J.-P. Lefaucheur, G. Mick, V. Piano, G. Pickering, E. Piquet, C. Regis, E. Salvat, N. Attal
Douleur et analgésie - Volume 33, numéro 2, Juin 2020 - DOI 10.3166/dea-2020-0113
La SFETD a élaboré des recommandations professionnelles concernant les douleurs neuropathiques chroniques (de durée au moins égale à trois mois) de l'adulte et de l'enfant. Ces recommandations sont destinées à l'ensemble des professionnels de santé confrontés aux douleurs neuropathiques en ambulatoire : généralistes, neurologues, rhumatologues, gériatres, odontologistes, kinésithérapeutes et infirmiers.
La douleur neuropathique (DN) est secondaire à une lésion ou à une maladie affectant le système nerveux somatosensoriel. Elle a un impact considérable sur la qualité de vie et est à l'origine d'un coût socio-économique majeur [1–4]. Cependant, de nombreux patients présentant une DN ne reçoivent pas de traitement pharmacologique approprié [2,5–9]. De nombreuses raisons peuvent être avancées, notamment une méconnaissance du diagnostic de DN ou un manque de connaissance des molécules efficaces et de leurs modalités d'utilisation. Par ailleurs, les approches non pharmacologiques telles que la neurostimulation, la psychothérapie et les techniques dites complémentaires (hypnose, acupuncture…) sont de plus en plus souvent proposées aux patients douloureux neuropathiques, simultanément ou successivement [10,11].
Cependant, les recommandations pour la prise en charge de la DN ont toujours été limitées à un type de traitement spécifique, notamment les traitements pharmacologiques ou la neurostimulation. Ainsi, les dernières recommandations françaises pour le traitement de la douleur neuropathique ont ciblé les approches pharmacologiques [12]. Depuis ces recommandations publiées en 2010, des recommandations internationales fondées sur les preuves ont été diffusées pour les traitements pharmacologiques [13], les techniques interventionnelles [14] et la neurostimulation centrale [15]. Aucune recommandation prenant en compte l'ensemble des techniques disponibles pour la prise en charge de la DN n'a été élaborée jusqu'à présent. De plus, la majorité des recommandations précédentes n'ont pris en compte que les études réalisées chez l'adulte, et pas les patients pédiatriques ou très âgés. En France, le traitement de la douleur neuropathique en pédiatrie est fondé sur les recommandations de l'AFFSSAPS de 2009 [16], qui sont principalement issues de recommandations faites chez l'adulte et d'avis d'experts.
Le présent document correspond à une version synthétique des nouvelles recommandations françaises publiées en langue anglaise en 2020, qui intègrent l'ensemble des options thérapeutiques disponibles pour la DN [17].
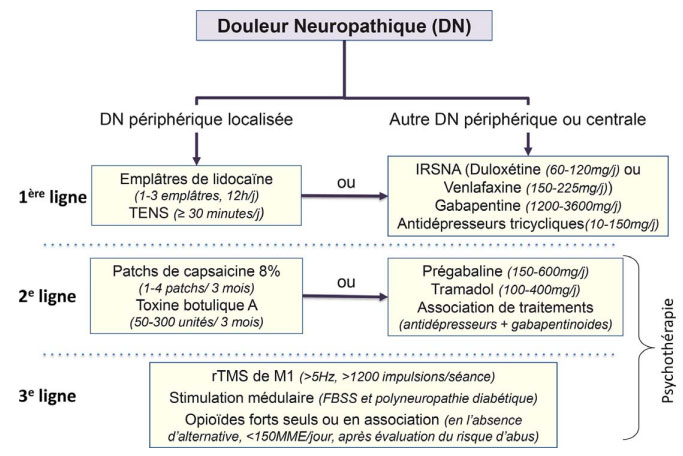
Ces traitements peuvent être utilisés seuls ou en association avec des traitements systémiques (consensus d'experts) et sont à favoriser chez des patients avec une zone douloureuse peu étendue et une sensibilité résiduelle de leur aire douloureuse (c'est-à-dire sans anesthésie totale à la stimulation thermique ou mécanique dans la zone douloureuse).
Ces 2 traitements sont disponibles uniquement en usage hospitalier (hôpital de jour pour la capsaïcine). Ces traitements peuvent être utilisés seuls ou en association avec des traitements systémiques (consensus d'experts) et sont à favoriser chez des patients avec une zone douloureuse peu étendue et avec une sensibilité résiduelle (c'est-à-dire sans anesthésie totale à la stimulation thermique ou mécanique dans la zone douloureuse) ainsi qu'une allodynie mécanique pour la toxine botulique.
Il est toujours important de débuter à faibles posologies et d'augmenter lentement les doses pour tous les traitements oraux afin de minimiser le risque d'effets indésirables. Les patients doivent être informés du risque de ces traitements pour la conduite automobile, en particulier lors de leur initiation.
Il est toujours important de débuter à faibles posologies et d'augmenter lentement les doses pour tous les traitements oraux afin de minimiser le risque d'effets indésirables. Les patients doivent être informés du risque de ces traitements pour la conduite automobile, en particulier lors de leur initiation.
Aucune étude n'a défini les règles de passage à un traitement de deuxième ou de troisième intention. En l'absence de contre-indication, les traitements de première intention devraient être proposés en premier. En cas d'effets indésirables non tolérables ou de manque d'efficacité, définis comme une diminution de la douleur de moins de 30 % et/ou une amélioration fonctionnelle de moins de 30 % après un essai d'au moins 6 semaines à la dose maximale tolérée, un changement pour un traitement de deuxième intention peut être proposé (consensus d'experts). La même règle peut s'appliquer pour passer de la deuxième à la troisième intention (consensus d'experts).
Légende :
Ces recommandations sont extraites de « Traitements pharmacologiques et non pharmacologiques de la douleur neuropathique : une synthèse des recommandations françaises » - X. Moisset, D. Bouhassira, J. Avez Couturier, H. Alchaar, S. Conradi, M.-H. Delmotte, M. Lantéri-Minet, J.-P. Lefaucheur, G. Mick, V. Piano, G. Pickering, E. Piquet, C. Regis, E. Salvat, N. Attal
Douleur et analgésie - Volume 33, numéro 2, Juin 2020 - DOI 10.3166/dea-2020-0113
Le questionnaire DN4 distingue les douleurs neuropathiques des autres types de douleur ou détecte une composante neuropathique dans des douleurs mixtes. Il a deux parties (interrogatoire + examen clinique).
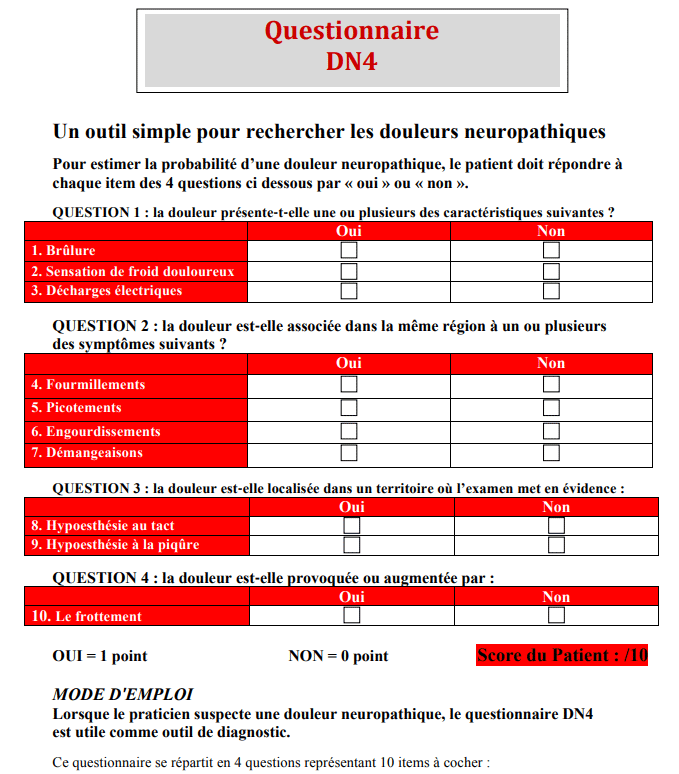
Télécharger le questionnaire DN4.

• Le National Institute of Health and care excellence (2020)
• L’académie Américaine de Neurologie (2021)
• La Société d’Endocrinologie, de Métabolisme et de Diabète d'Afrique (2017)
| Prégabaline | Gabapentine | |
|---|---|---|
| Tmax | Dans l'heure | 3 à 4 heures |
| Absorption | rapide | lente |
| Biodisponibilité orale |
jusqu'à 90% | jusqu'à 60% |
| Concentration plasmatique |
linéaire | non-linéaire |
| Puissance | 2,8 fois plus puissante que la Gabapentine | - |
| Posologie | 2 à 3 fois/jour (max 600 mg/jour) |
3 à 4 fois/jour (max 3600 mg/jour) |

Consultez le RCP de Striprega® 75 mg

Consultez le RCP de Striprega® 150 mg
Nous vous invitons à nous signaler tout effet indésirable concernant nos produits : Pharmacovigilance Strides

Consultez les RCP de toutes les formes et présentations de nos produits disponibles dans votre pays dans le Dictionnaire Internet Africain des Médicaments (DIAM)


Chaque gélule de gélatine dure contient : Prégabaline : 75 mg.
Chaque gélule de gélatine dure contient : Prégabaline : 150 mg.
Excipient à effet notoire : lactose monohydraté.
Gélule de gélatine dure.
Utilisation par voie orale.
La gamme posologique est de 150 à 600 mg par jour, administrés en deux ou trois doses fractionnées.
Le traitement par prégabaline peul être initié à une dose de 150 mg par jour. Sur la base de la réponse et de la tolérance du patient individuel, la dose peut être augmentée à 300 mg par jour après 1 semaine. Après une semaine supplémentaire, la dose peut être augmentée à 450 mg par jour. La dose maximale de 600 mg par jour peut être atteinte après une semaine supplémentaire.
| Indications | Schéma posologique | Dose maximale |
|---|---|---|
| Douleur associée à la NPD | 3 doses divisées par jour | 300 mg/jour en 1 semaine |
| NPZ | 2 ou 3 doses divisées par jour | 300 mg/jour en 1 semaine Maximum 600 mg/jour |
| Traitement d'appoint pour le traitement des crises partielles chez les patients âgés de 4 ans et plus | 2 ou 3 doses divisées par jour | Maximum 600 mg/jour |
| Fibromyalgie | 2 doses divisées par jour | 300 mg/jour en 1 semaine Maximum 450 mg/jour |
| Douleur neuropathique associée à une lésion médullaire | 2 doses divisées par jour | 300 mg/jour en 1 semaine Maximum 600 mg/jour |
| Trouble d'anxiété généralisé | 2 ou 3 doses divisées | 300 mg/jour en 1 semaine Maximum 600 mg/jour |
Conformément à la pratique clinique en vigueur, si le traitement par prégabaline doit être arrêté, il est recommandé de le faire progressivement, sur une durée d'une semaine au minimum, indépendamment de l'indication.
La prégabaline est éliminée de la circulation systémique principalement par excrétion rénale sous forme inchangée. Étant donné que la clairance de la prégabaline est directement proportionnelle à la clairance de la créatinine, la réduction de la dose des patients présentant une fonction rénale compromise doit être individualisée en fonction de la clairance de la créatinine (Cler).
La prégabaline est éliminée efficacement du plasma par hémodialyse (50% du médicament en 4 heures). Pour les patients sous hémodialyse, la posologie quotidienne de Prégabaline doit être ajustée en fonction de la fonction rénale. En plus de la dose quotidienne, une dose supplémentaire doit être administrée immédiatement après chaque séance d'hémodialyse de 4 heures.
| Clairance de la créatinine (Cler) (ml/min) | Dose quotidienne totale de prégabaline* | Schéma posologique | |
|---|---|---|---|
| Dose de départ (mg/jour) | Dose maximale (mg/jour) | ||
| ≥ 60 | 150 | 600 | BID ou TID |
| ≥ 30 - < 60 | 75 | 300 | BID ou TID |
| ≥ 15 - < 30 | 25 - 50 | 160 | Une fois par jour ou BID |
| > 15 | 25 | 75 | Une fois par jour |
| Posologie supplémentaire après l'hémodialyse (mg) | |||
| 25 | 100 | Dose unique* | |
TID =Trois doses divisées BIO= Deux doses divisées.
* La dose quotidienne totale (mg/jour) doit être fractionnée comme indiqué par le schéma posologique afin de fournir mg/ dose
+ Une dose supplémentaire est une dose supplémentaire unique
Aucun ajustement posologique n'est nécessaire chez les patients présentant une insuffisance hépatique.
La sécurité et l'efficacité de la Prégabaline chez les enfants de moins de 12 ans et chez les adolescents (12 à 17 ans) n'ont pas été établies.
Les patients âgés peuvent avoir besoin d'une réduction de la dose de prégabaline en raison d'une diminution de la fonction rénale.
La Prégabaline peut être prise avec ou sans nourriture. La Prégabaline est pour une utilisation par voie orale uniquement.
Les capsules de prégabaline sont contre-indiquées chez les patients présentant une hypersensibilité connue à la prégabaline ou à l'un de ses composants. Des cas d'oedème de Quincke et des réactions d'hypersensibilité se sont produits chez des patients recevant un traitement par prégabaline.
Un oedème de Quincke et une hypersensibilité peuvent se produire. Interrompre progressivement le traitement par Prégabaline afin de minimiser le risque d'une augmentation de la fréquence des crises chez les patients présentant des troubles convulsifs. Augmente le risque d'idées et de comportements suicidaires. Peut provoquer un oedème périphérique, des étourdissements, de la somnolence et une prise de poids. Suivant un arrêt soudain et rapide, des patients ont rapportés des symptômes incluant : insomnie, nausées, mal de tête et diarrhée. Réduire progressivement sur une durée minimale d'une semaine. Une incidence élevée d'hémangiosarcome a été identifiée dans deux souches différentes de souris lors de l'administration de prégabaline. La signification clinique de cette observation est inconnue.
Il faut conseiller aux patients d'informer leur médecin si des changements dans la vision se produisent.
Arrêter le traiter par prégabaline si une myopathie est diagnostiquée ou soupçonnée ou si des taux de créatinine kinase considérablement élevés sont observés.
Peut provoquer une diminution de la numération plaquettaire et un allongement de l'intervalle PR.
Étant donné que la Prégabaline est principalement excrétée sous forme inchangée dans l'urine, est très faiblement métabolisée chez les humains (< 2% d'une dose retrouvée dans l'urine sous forme de métabolites), n'inhibe pas le métabolisme du médicament in vitro, et n'est pas liée aux protéines plasmatiques, elle est peu susceptible de produire d'être sujet à des interactions pharmacocinéliques.
En conséquence, dans les études in vivo, aucune interaction pharmacocinétique cliniquement pertinente n'a été observée entre la Prégabaline et la phénytoïne, la carbamazépine, l'acide valproïque, la lamotrigine, la gabapentine, le lorazépam, l'oxycodone ou l'éthanol. L'analyse pharmacocinétique de population a indiqué que les antidiabétiques oraux, les diurétiques, l'insuline, le phénobarbital, la tiagabine et le topiramate n'avaient aucun effet cliniquement significatif sur la clairance de la Prégabaline.
La co-administration de prégabaline avec des contraceptifs oraux tels que la norélhislérone et / ou l'éthinylestradiol n'influence pas la pharmacocinélique à l'état d'équilibre de l'une ou l'autre substance.
La prégabaline peut potentialiser les effets de l'éthanol et du lorazépam. Dans les essais cliniques contrôlés, la co-administration de doses orales multiples de Prégabaline avec de l'oxycodone, du lorazépam ou de l'éthanol n'a pas entraîné d'effets cliniquement importants sur la respiration. Au cours de l'expérience postcommercialisation, des cas d'insuffisance respiratoire et de coma ont été rapportés chez des patients qui prenaient de la prégabaline et d'autres médicaments dépresseurs du SNC. La prégabaline semble être additive dans l'altération de la fonction cognitive et la motricité globale causée par l'oxycodone.
Les médicaments antiépileptiques peuvent affecter le développement du fœtus tout au long de la grossesse. Compte tenu des indications thérapeutiques générales de la prégabaline (PGB) et de ses effets tératogènes potentiels, il est conseillé d'éviter ce médicament pendant la grossesse.
On ne sait pas si la prégabaline est excrétée dans le lait maternel des humains ; cependant, elle est présente dans le lait des rates. Par conséquent, l'allaitement est déconseillé pendant le traitement par prégabaline
Les effets indésirables fréquents de la prégabaline sont : étourdissements, somnolence, sécheresse buccale, œdème, vision trouble, prise de poids, et « pensées anormales » (principalement un problème de concentration/ d'attention).
La prégabaline semble être relativement bénigne en cas de surdosage. Un cas de surdosage où 8 grammes de Prégabaline ont été pris sans aucun effet clinique inattendu, ainsi qu'un cas de surdosage de 11,5 grammes avec des conséquences plus graves ont été rapportés. Des soins généraux de soutien sont indiqués, et en cas de surdosage, les effets indésirables suivants peuvent se produire : agitation, coma, convulsions, suppression hémopoïétique, tachycardie sinusale et rétention urinaire. Il n'existe aucun antidote spécifique pour les surdosages de Prégabaline. Si indiqué, l'élimination du médicament non absorbé devrait être tentée par des vomissements ou un lavage gastrique ; les précautions habituelles doivent être respectées afin de maintenir les voies respiratoires.
Des soins généraux de soutien sont indiqués, de même qu'une surveillance des signes vitaux et une observation de l'état clinique du patient.
Bien que l'hémodialyse n'ait pas été effectuée dans les quelques cas connus de surdosage, elle peut être indiquée en fonction de l'état clinique du patient ou chez les patients présentant une insuffisance rénale significative. Les procédures d'hémodialyse standard entraînent une clairance importante de la prégabaline (environ en 4 heures).
La prégabaline se lie avec une grande affinité au site alpha-2-delta (sous-unité auxiliaire des canaux calciques dépendants du voltage) dans les tissus du système nerveux central.
Bien que le mécanisme d'action de la prégabaline soit inconnu, les résultats obtenus avec des souris génétiquement modifiées et avec des composés structurellement apparentés à la prégabaline (comme la gabapentine) suggèrent que la liaison à la sous-unité alpha-delta pourrait être impliquée dans les effets antinociceptifs et anti-crises de la prégabaline dans les modèles animaux.
ln vitro, la prégabaline réduit la libération dépendante du calcium de plusieurs neurotransmetteurs, probablement à travers la modulation de la fonction des canaux calciques. Bien que la prégabaline soit un dérivé structurel de l'acide gammaaminobutyrique (GABA), un neurotransmetteur inhibiteur, elle ne se lie pas directement aux récepteurs du GABA (A), du GABA (B) ou des benzodiazépines, n'augmente pas les réponses du GABA (A) dans les neurones en culture, n'altère pas la concentration de GABA dans le cerveau des rats et n'a pas d'effets aigus sur l'absorption ou la dégradation du GABA.
Cependant, dans les neurones en culture, l'application prolongée de prégabaline augmente la densité de la protéine du transporteur GABA et augmente le taux de transport fonctionnel de GABA. La prégabaline ne bloque pas les canaux sodiques, n'est pas active au niveau des récepteurs opiacés et n'altère pas l'activité de l'enzyme cyclooxygénase. Elle est inactive au niveau des récepteurs de la sérotonine et de la dopamine et n'inhibe pas la recapture de la dopamine, de la sérotonine ou de la noradrénaline.
La prégabaline est bien absorbée après son administration par voie orale.
Elle est largement éliminée par excrétion rénale.
Sa demi-vie d'élimination est d'environ 6 heures.
Après l'administration orale de capsules de prégabaline à jeun, les concentrations plasmatiques maximales sont atteintes en 1,5 heure. La biodisponibilité orale de la prégabaline est égale à 90% et est indépendante de la dose. Après l'administration d'une dose unique (25 à 300 mg) et de doses multiples (75 à 900 mg/jour), les valeurs de la concentration plasmatique maximale (Cmax) et de l'aire sous la courbe de la concentration plasmatique en fonction du temps (ASC) augmentent de façon linéaire. Après l'administration répétée, l'état d'équilibre est atteint dans les 24 à 48 heures.
La pharmacocinélique des doses multiples peut être prédite à partir des données suries doses uniques.
Le taux d'absorption de prégabaline est réduit lorsqu'elle est administrée avec de la nourriture, ce qui entraîne une diminution de la Cmax d'environ 25% à 30% et une augmentation du tmax d'environ 3 heures. Cependant, l'administration de Prégabaline avec de la nourriture n'a aucun effet cliniquement pertinent sur l'absorption totale de la prégabaline. Par conséquent, la prégabaline peut être prise avec ou sans nourriture. La prégabaline ne se lie pas aux protéines plasmatiques. Le volume apparent de distribution de la Prégabaline après l'administration orale est d'environ 0,5 L/kg.
La prégabaline est un substrat du transporteur du système L qui est responsable du transport de grands acides aminés à travers la barrière cérébrale. Bien qu'il n'existe aucune donnée chez les humains, il a été démontré que la prégabaline traverse le placenta chez les rats et est présente dans le lait des rates en lactation.
La prégabaline est très faiblement métabolisée chez les humains. Après une dose de prégabaline radio-marquée, environ 90% de la dose administrée a été retrouvée dans l'urine sous forme de prégabaline inchangée. Le dérivé N-mélhylé de la Prégabaline, le principal métabolite de la Prégabaline présent dans l'urine, représentait 0,9% de la dose. Au cours des études précliniques, la prégabaline {énantiomère S) n'a pas subi de racémisation en énantiomère R chez la souris, les rats, les lapins ou les singes.
La prégabaline est éliminée de la circulation systémique principalement par excrétion rénale sous forme de médicament inchangé avec une demi-vie d'élimination moyenne de 6,3 heures chez les sujets présentant une fonction rénale normale. Il a été estimé que la clairance rénale moyenne était entre 67,0 et 80,9 ml/min chez les jeunes sujets en bonne santé.
Étant donné que la prégabaline n'est pas liée aux protéines plasmatiques, ce taux de clairance indique qu'une réabsorption tubulaire rénale est impliquée.
L'élimination est presque proportionnelle à la clairance de la créatinine.
Conserver à une température inférieure à 30°C. Protéger de la lumière et de l'humidité. Garder le médicament hors de la portée des enfants.
Durée de vie : 24 mois
Conditionnement :
Strides Pharma Science Limited
Strides House, Opp IIM-B, Bilekahalli,
Bannerghatta Road,
Bangalore – 560076, India
Dernière mise à jour de cette page
02/05/2025.
Liste I.
![]() Adresse
Adresse
![]() Téléphone
Téléphone
Revue MAF
Revue OST
Actualités
Rubriques spécialités
Webinaires
Espaces labos